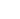类器官,顾名思义是人体真实器官及生理系统的模拟,作为干细胞研究的重要成果之一,对于临床精准医疗(为患者制定个体化治疗方案)、临床前药物研发等有着非凡价值;因此也成为TOP药企必须拿下的据点。
而在这一辉瑞、艾伯维、强生、罗氏、默沙东、诺华、BMS、赛诺菲、GSK、阿斯利康、武田制药等全球TOP20药企都在争相布局的未来领域,已经有企业拔得头筹。
近日,FDA批准了全球首个完全基于“类器官芯片”研究获得临床前数据的新药(NCT04658472)进入临床试验。这一里程碑事件,意味着“类器官芯片”实验首次取代了传统动物实验,并且正式被官方认可。
这项新药实验由赛诺菲和类器官芯片公司Hesperos合作进行,用于治疗两种罕见的自身免疫性脱髓鞘神经疾病,而在此之前,由于缺乏理想的动物模型,无法针对这些疾病开展研究。
至此,赛诺菲后来居上,虽不是第一个布局,但在“类器官”实践领域超前全场。
如果该项目进展顺利,或将彻底颠覆临床开发的种种限制,改变全球药物研发的游戏规则
全球类器官相关临床试验注册
前几日,全球制药巨头Roche宣布成立Institute of Human Biology(IHB,人类生物学研究所),押注类器官(Organoids)等模型,旨在利用这些模型的优势,缩短药物研发周期,提高新药研发成功率。去年圣诞节前夕,美国众议院批准了FDA现代法案2.0,该法案将允许新药不需要在动物上进行实验也能获得美国FDA的批准,为类器官带来了契机。
目前,全球范围内众多药企,医院,高校课题组都在积极开展类器官底层技术创新及相关应用,旨在加速类器官技术实现临床转化。
以“Organoid”、“类器官”为关键词分别在美国临床试验注册中心和中国临床试验注册中心搜索数据。自2008年至今,在美注册类器官相关临床试验数量共计169项;在中国注册类器官相关临床试验数据共计44项。
从2017年开始,两地类器官相关临床试验注册数量陡增,2018年类器官技术被Nature Motheds评为“2017年度方法”,随后在2019年被新英格兰杂志评为“优良的人类临床前疾病模型”。
第一项类器官临床试验注册于2008年(NCT00646022),名为“Natural History of Familial Carcinoid Tumor”,目前状态仍为“招募中”,最近一次更新于上个月初。
该试验将招募1600名受试者,旨在通过评估具有肠癌家族史的人群,提高肠癌早期检测率,并发现潜在肿瘤相关性基因。该实验的次要目标包含了建立肠道类器官。
类器官的一大分支为肿瘤类器官。肿瘤类器官由患者肿瘤组织培养而来,保留了个体肿瘤的异质性,且组织结构、细胞类型和基因特征与来源组织高度一致。
乳腺癌、肺癌、结直肠癌为全球前三大癌种,小编整理分析了中美两地注册的213项临床试验中与以上三个癌种相关的试验(此处以肠癌作为统计)。
两地注册的临床试验中,肠癌相关项目数量均为最多,在美注册26项,在国内注册5项。肠道肿瘤类器官临床研究数量的领先,或许可以归功于肠道肿瘤类器官是第一个被建立的肿瘤类器官:2011年,Sato等运用类器官技术率先建立了肿瘤类器官,他们在小鼠结肠隐窝的培养条件的基础上,通过优化调整培养条件,从结肠腺瘤和腺癌及Barrett食管中建立肿瘤类器官模型。
三个癌种在美共计注册59项,占注册总数的34.91%;在国内共计注册10项,占注册总数的22.73%。
值得注意的是,在美注册的以上三个癌种相关临床试验中,处于临床1期的试验有5个(包含Early phase1,Phase1/Phase2),处于临床2期的试验有10个(一个已终止),处于临床3期的有2个(一个已撤回)。预计纳入研究的受试者总数为9961人。这些研究引入类器官技术的目的以探索药物敏感性、药效评价为主。
新技术的转化成效,在临床试验中的应用是一个考量维度。
目前,唯一在研的类器官相关的临床3期试验题为“Precise Therapy for Refractory HER2 Positive Advanced Breast Cancer(精准治疗难治性HER2阳性晚期乳腺癌)”(NCT05429684),发起单位为西安交通大学第一附属医院。
这是一项开放性、前瞻性和干预性的临床研究,入组人群为对曲妥珠单抗耐药的晚期HER2阳性乳腺癌患者。
研究人员将采集活检组织并构建PDO模型。患者及其组织衍生的PDO模型根据基因组特征被分为六组,每组患者将接受最佳的针对性治疗方案,而配对的PDO模型将接受各种潜在的有效方案干预。根据药物对PDO的抑制率,及时调整患者的未来治疗方案。该研究的主要终点为ORR和PDO抑制率,次要终点为PFS1。
基于肿瘤类器官的药敏检测以指导临床药用为肿瘤类器官的一大发展方向,在新药研发早期阶段,肿瘤类器官也同样大有可为。
全球市场:TOP20药企均已直接入场
目前全球类器官芯片市场商业化主要来源于两方面:设备销售和测试服务;年复合增长率29%左右;美国市场占比最大约41%,欧洲约38%。
作为新药研发的重要助力,类器官芯片公司的下游客户主要包括CRO和药企。
类器官鼻祖Hans Clevers团队成立的HubrechtOrganoid Technology(HUB)是全球首个类器官研发中心,而HUB通过技术授权也助力了Epistem、Cellesce、Crown Biosciences、STEMCELL Technologies等第一批类器官公司涌现。
此外,高校研究院成立的技术公司也是这一类器官芯片公司的主力,例如哈佛大学Wyss生物工程学院2013年成立的生物技术公司Emulate。
此前类器官芯片企业大多通过向CRO出售产品间接为药企提供服务。2015年以后,越来越多的药企通过购买产品、合作授权以及投资等形式直接入场,成为这一领域的另一股力量。
2015年,强生购买Emulate公司的血栓芯片,用于检测其在已上市药物或在研药物中的促血凝特性。
2016年,默克、Seres Therapeutics等购买Emulate公司类器官芯片用于新药研发测试。
2018年,阿斯利康与Emulate公司达成协议,将其类器官芯片技术结合到阿斯利康的IMED药物安全实验室中;阿斯利康也是首家将类器官芯片技术整合进内部实验室的TOP药企。
2018年5月,辉瑞与HUB合作开发人类肠道类器官平台,用来研究克罗恩病、溃疡性结肠炎等疾病。
2018年9月,由辉瑞领投的神经治疗初创公司System1 Biosciences获2500万美元A轮融资,其自研大脑类器官,用于研发神经治疗新方法。
2021年,赛诺菲与Hesperos合作,共同进行NCT04658472临床前研究。
2022年1月,百时美施贵宝与Prellis 达成合作,基于其人体淋巴结类器官平台创建针对人类蛋白质的高亲和力人类抗体。
2022年3月,赛诺菲与Prellis达成合作,利用其平台在体外重建免疫反应以提供具有显着遗传多样性的抗体。
此外,由艾伯维、默克、诺华等20余家TOP药企共同成立非营利组织IQ联盟(Innovationand Quality Consortium),致力于推动类器官芯片的标准化应用,以加速药物研发进程。目前已针对肝脏、肾脏、肺等模型发表一系列行业标准。
中国市场:恒瑞、百济;罗氏、默克已领先布局
从2021年起,中国正式从科研和监管层面系统性推进类器官芯片技术的发展。
2021年1月28日,科技部下发《关于对“十四五”国家重点研发计划6个重点专项2021年度项目申报指南征求意见的通知》,把“基于类器官的恶性肿瘤疾病模型”列为“十四五”国家重点研发计划中首批启动重点专项任务。
2021年11月,中国CDE首次将类器官列入基因治疗及细胞治疗的验证指南基因治疗产品非临床药理学研究。
2022年7月,中国首个类器官指导肿瘤精准药物治疗的专家共识面世。
中国类器官芯片发展虽然比美国完了约十年,但是进步速度飞快。
中国科研积累的提升加速相关产业化进程。
2009-2019,在类器官技术相关领域来自于中国的发表文献占8%,位于全球第6;到2020年,来自中国的发表文献已达14%,仅次于美国,位于全球第2。
中国资本市场开始关注类器官企业。
从2019年开始,中国类器官企业开始赢得资本关注,纷纷完成天使轮融资,2021年完成A轮融资,
创芯国际完成近亿元A轮融资,由趣道资产领投;
丹望医疗完成1.2亿元A轮融资,由国方资本领投,德联资本、昆仑资本跟投,并且类器官“鼻祖”Hans Clevers以联合创始人和首席顾问科学家身份加盟;
大橡科技完成数千万元的A轮融资,由鼎晖VGC(鼎晖创新与成长基金)领投,奇绩创坛跟投,老股东药明康德、复容投资及久友资本继续跟投;
从药企来看,中国研发“一哥”和曾经的研发“一哥”都已布局类器官相关领域。
百济神州是IQ联盟里唯一的中国药企,2021年12月,其与创芯国际签署战略合作协议,共同建立类器官新药研发技术平台。
恒瑞医药的转化医学部门,建立了体外类器官培养(organoid culture),可以在模拟的人体器官及肿瘤微环境中进行药物研究;
跨国药企也将中国创新中心项目拓展至“类器官”相关领域。
2020年,默克中国创新中心开始探索创新“类器官”平台。
罗氏中国药物科学部门的重点项目之一是将人体模型系统(类器官和微生理系统)应用到药物发现产品管线中
注:文章来源于网络,如有侵权,请联系删除




 全部商品分类
全部商品分类