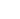来源:国家药监局医疗器械技术审评中心
8月23日,国家药监局医疗器械技术审评中心发布《创新医疗器械特别审查申请审查结果公示(2023年第6号)》。
《公示》披露,依据国家药品监督管理局《创新医疗器械特别审查程序》(国家药监局2018年第83号公告)要求,创新医疗器械审查办公室组织有关专家对创新医疗器械特别审查申请进行了审查,拟同意以下9款项目进入特别审查程序,分别为:
1.产品名称:心脏冷冻消融系统申请人:上海安钛克医疗科技有限公司
2.产品名称:植入式心脏复律除颤器申请人:苏州无双医疗设备有限公司
3.产品名称:一次性使用压力监测脉冲电场消融导管申请人:四川锦江电子医疗器械科技股份有限公司
4.产品名称:一次性使用磁电定位压力监测脉冲电场消融导管申请人:湖南埃普特医疗器械有限公司
5.产品名称:脉冲电场消融设备申请人:深圳迈微医疗科技有限公司
6.产品名称:近红外光脑功能治疗仪申请人:丹阳慧创医疗设备有限公司
7.产品名称:颅内动脉瘤介入手术仿真软件申请人:西姆医疗公司
8.产品名称:人CDO1/AJAP1/GALR1基因甲基化检测试剂盒(荧光PCR法)申请人:武汉凯德维斯生物技术有限公司
9.产品名称:光固化创面封闭胶申请人:中山光禾医疗科技有限公司
公示时间:2023年8月23日至2023年9月6日
注:文章来源于网络,如有侵权,请联系删除




 全部商品分类
全部商品分类