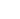5月13日,葛兰素史克宣布,其HIV药物专研合资公司ViiV Healthcare卡替拉韦钠片和卡替拉韦注射液近日同时获得中国国家药品监督管理局批准,用于有感染风险的成人和青少年(体重≥35kg)进行HIV-1暴露前预防(PrEP),以降低性传播感染HIV-1的风险,结合安全的性行为措施以达到更好的HIV-1 PrEP效果。美国FDA在2021年12月20日官方新闻稿中指出,它是首个无需每日服药就能预防HIV感染的疗法。
HIV是指艾滋病,又称为获得性免疫缺陷综合征(AIDS),是由于机体感染人类免疫缺陷病毒(HIV),亦称艾滋病病毒,而引发的全身性疾病。艾滋病病毒感染可导致人体不同程度的免疫功能缺陷,未经治疗的感染者在疾病晚期易于并发各种严重感染和恶性肿瘤,最终导致死亡。
艾滋病是全球共同面临的重大公共卫生问题之一,现存约3900万HIV感染者。截至2023年年底,中国存活艾滋病患者及病毒感染者129万人。联合国艾滋病规划署提出到2025年,要实现全球95%有HIV感染风险的人群接受有效、综合的预防措施的目标与承诺,因此预防HIV新发感染已成为防控艾滋病传播的关键。
暴露前预防(pre-exposure prophylaxis, PrEP)是通过使用抗病毒药物来预防HIV感染的一种有效的生物学预防方法。作为一种HIV-1整合酶链转移抑制剂(INSTI),卡替拉韦长效方案仅需每年注射最少6次即可实现HIV暴露前预防。使用者将在前两个月内接受每月600mg(3ml)的起始注射,随后每两个月接受一次600mg(3ml)的继续注射。在首次注射前,使用者可选择先口服卡替拉韦钠片剂大约一个月(至少28天),以评估药物的耐受性。
据了解,此次获批的HIV暴露前预防长效药物是基于两项国际IIb/III期多中心、随机、双盲、阳性对照研究(HPTN 083和HPTN 084),旨在评估卡替拉韦长效注射液对于HIV-1阴性男男同性性行为者、跨性别女性及顺性别女性HIV暴露前预防的安全性和有效性。HPTN 083研究结果显示,与每日口服富马酸替诺福韦二吡呋酯/恩曲他滨(TDF/FTC)方案相比,接受卡替拉韦长效注射液的参与者感染HIV的风险降低了68%(12vs39; 年发病率:0.37%vs1.22%;HR0.32[CI:0.16,0.58])。HPTN084研究结果显示,相较于TDF/FTC口服片剂组,长效注射液组的HIV感染风险降低91%(3vs36;年发病率:0.15%vs1.85%;HR0.09[CI:0.04,0.27])。
注:文章来源于网络,如有侵权,请联系删除




 全部商品分类
全部商品分类